Биология - ВИЧ - ВИЧ-инфекция
09 февраля 2011Оглавление:
1. ВИЧ
2. История открытия
3. Биология ВИЧ
4. ВИЧ-инфекция
5. Эпидемиология
6. Анти-ВИЧ-кремы и гели
7. Юридические последствия заражения другого человека ВИЧ-инфекцией
ВИЧ-инфекция — вирусное заболевание, вызываемое вирусом иммунодефицита человека. Последней стадией заболевания является СПИД.
Период от инфицирования вирусом иммунодефицита человека до развития СПИД длится в среднем 9 — 11 лет . Статистические данные многочисленных исследований, проведённых в различных странах за период времени более двух десятилетий, подтверждают это заключение. Эти цифры справедливы лишь для случаев, когда ВИЧ-инфекция не подвергается никакой терапии.
Группы риска
Группы повышенного риска:
- лица, употребляющие инъекционные наркотики, использующие общую посуду для приготовления наркотика; а также их половые партнёры.
- лица, практикующие незащищённый анальный секс
- лица, практикующие незащищённый вагинальный секс
- лица, которым сделали переливание непроверенной донорской крови;
- врачи;
- больные другими венерическими заболеваниями;
- коммерческие секс-работники и их клиенты
Патогенез
Основа патогенеза ВИЧ до сих пор не очень ясна. Последние данные говорят о том, что гиперактивация иммунной системы в ответ на инфекцию является основным фактором патогенеза ВИЧ. Одной из черт патогенеза является гибель CD4+ Т-клеток, концентрация которых медленно, но неуклонно снижается. Также снижается количество дендритных клеток, профессиональных антиген-презентирующих клеток, которые в основном и начинают иммунный ответ к патогену, что по важности последствий для иммунной системы является может даже более сильным фактором, нежели гибель Т-хелперов. Причины гибели дендритных клеток остаются неясными.
Некоторые причины гибели хелперов:
- Взрывная репродукция вируса.
- Слияние мембран заражённых и незаражённых хелперов с образованием нежизнеспособных симпластов. Симпласты были обнаружены только в лабораторных условиях в условиях культур клеток.
- Атака заражённых клеток цитотоксичными лимфоцитами.
- Адсорбция свободного gp120 на CD4+ незаражённых хелперах с их последующей атакой цитотоксических лимфоцитов.
Основной причиной гибели Т-клеток при ВИЧ-инфекции является программируемая клеточная гибель. Даже на стадии СПИД уровень инфицированности Т4-клеток составляет 1:1000, что говорит о том, что вирус сам по себе не способен убить такое количество клеток, которое погибает при ВИЧ-инфекции. Также не объяснить столь массовую гибель Т-клеток и цитотоксическим действием других клеток.
Нарушения в работе иммунной системы со временем нарастают вплоть до полной неспособности осуществлять свою основную функцию — защиту организма от болезнетворных организмов. На фоне гиперактивации часто возникают лейкозы, что в совокупности приводит к тому, что факультативные паразиты, которые сосуществуют в здоровом организме под контролем иммунной системы, выходят из под контроля, становясь гибельными для организма.
Основной резервуар ВИЧ в организме — макрофаги и моноциты:
- В них не происходит взрывающей репродукции.
- Выход происходит через комплекс Гольджи.
Стадии инфекционного процесса
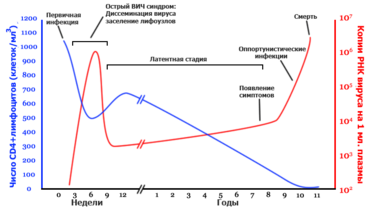
Число копий РНК вируса на мл. плазмы
Общая продолжительность составляет в среднем 10 лет. В течение всего этого времени наблюдается постоянное снижение количества лимфоцитов в крови больного, что в конечном итоге становится причиной смерти.
Инкубационный период — от 3-х недель до 3 месяцев.
Продромальный период — стадия первичного инфицирования, до 1 месяца. Клинические проявления: субфебрильная температура, крапивница, стоматит, воспаление лимфатических узлов — они становятся увеличенными, мягкими и болезненными. Максимальная концентрация вируса, антител появляется только в самом конце продромального периода.
Латентный период — 5-10 лет, единственное проявление — стойкое увеличение лимфатических узлов — лимфоаденопатия.
ПреСПИД — продолжительность 1-2 года — начало угнетения клеточного иммунитета. Часто рецидивирующий герпес — долго не заживающие изъязвления слизистой рта, половых органов, стоматит. Лейкоплакия языка. Кандидоз — слизистой рта, половых органов.
Терминальная стадия — СПИД — 1-2 года.
Генерализация оппортунистических инфекций и опухолей.
- заболевание туберкулёзом
- сальмонеллы — переход в генерализованную форму, энцефалит, менингит.
- Legionella pneumophyla
- все вирусы гриппа, вирус простого герпеса.
- простейшие — криптоспоригии, токсоплазма
- грибы — кандида, гистоплазма, криптококк, плесневые грибы.
- злокачественные опухоли.
- саркома Капоши.
- лимфомы.
- пневмоцистная пневмония
Диагностика
Течение ВИЧ-инфекции характеризуется длительным отсутствием существенных симптомов болезни . Диагноз ВИЧ-инфекции ставится на основании лабораторных данных: при выявлении в крови антител к ВИЧ. Антитела к ВИЧ в период острой фазы, как правило, не обнаруживают. В первые 3 мес. после заражения антитела к ВИЧ выявляются у 96-97 % пациентов, через 6 мес. — у остальных 2-3 %, а в более поздние сроки — только у 0,5-1 %. В стадии СПИД регистрируют существенное снижение содержания антител в крови. Первые недели после инфицирования представляют собой «период серонегативного окна», когда антитела к ВИЧ не выявляются. Поэтому отрицательный результат тестирования на ВИЧ в этот период не означает, что человек не инфицирован ВИЧ и не может заразить других.
Для диагностики поражения слизистой оболочки рта у ВИЧ-инфицированных больных принята рабочая классификация, утверждённая в Лондоне, в сентябре 1992 года. Все поражения разделены на 3 группы:
- 1 группа — поражения, чётко связанные с ВИЧ-инфекцией. В эту группу включены следующие нозологические формы:
- кандидозы;
- волосистая лейкоплакия;
- маргинальный гингивит;
- язвенно-некротический гингивит;
- деструктивный пародонтит;
- саркома Капоши;
- неходжкинская лимфома.
- 2 группа — поражения, менее чётко связанные с ВИЧ-инфекцией:
- бактериальные инфекции;
- болезни слюнных желёз;
- вирусные инфекции;
- тромбоцитопеническая пурпура.
- 3 группа — поражения, которые могут быть при ВИЧ-инфекции, но не связанные с нею.
Наибольший интерес вызывают и наиболее часто встречаются поражения, относящиеся к 1 группе.
В России при постановке диагноза ВИЧ-инфекция проводится дотестовое и послетестовое консультирование пациента, разъяснение основных фактов о заболевании. Пациенту предлагается встать на учет в территориальный центр профилактики и борьбы со СПИД для бесплатного диспансерного наблюдения врачом-инфекционистом. Приблизительно раз в полгода рекомендуется сдавать анализы для контроля состояния здоровья. В случае значительного ухудшения этих показателей рекомендуется прием антиретровирусных препаратов.
Терапия
До настоящего времени не разработано лечения ВИЧ-инфекции, которое могло бы устранить ВИЧ из организма.
Современный способ лечения ВИЧ-инфекции замедляет и практически останавливает прогрессирование ВИЧ-инфекции и её переход в стадию СПИД, позволяя ВИЧ-инфицированному человеку жить полноценной жизнью. При использовании лечения и при условии, что эффективность лекарств сохраняется, продолжительность жизни человека ограничивается не ВИЧ, а лишь естественными процессами старения. Однако после длительного использования одной и той же схемы терапии, через несколько лет, вирус мутирует, приобретая резистентность к применяемым препаратам, и для дальнейшего контроля над прогрессированием ВИЧ-инфекции необходимо применять новые схемы лечения с другими препаратами. Поэтому любая существующая на сегодняшний день схема лечения ВИЧ-инфекции рано или поздно становится неэффективной. Также, во многих случаях, пациент не может принимать отдельные препараты по причине индивидуальной непереносимости. Поэтому грамотное применение терапии отсрочивает развитие СПИД на неопределенное время. На сегодняшний день появление новых классов препаратов в основном нацелено на уменьшение побочных эффектов от приема терапии, поскольку продолжительность жизни ВИЧ-положительных людей, принимающих терапию, практически сравнялась с продолжительностью жизни ВИЧ-отрицательного населения. В период более позднего развития ВААРТ выживаемость ВИЧ-инфицированных больных при исключении больных с гепатитом С достигает 38,9 лет.
Важное значение придается поддержанию здоровья ВИЧ-положительного немедикаментозными средствами, а также регулярный мониторинг состояния здоровья у врачей-специалистов по ВИЧ.
Устойчивость к ВИЧ
Несколько лет назад был описан генотип человека, устойчивый к ВИЧ. Проникновение вируса в иммунную клетку связано с его взаимодействием с поверхностным рецептором: белком CCR5. Но делеция CCR5-дельта32 приводит к невосприимчивости её носителя к ВИЧ. Предполагается, что эта мутация возникла примерно две с половиной тысячи лет назад и со временем распространилась в Европе.
Сейчас к ВИЧ фактически устойчив в среднем 1 % европейцев, 10-15 % европейцев имеют частичную сопротивляемость к ВИЧ.
Учёные Ливерпульского университета объясняют такую неравномерность тем, что мутация CCR5 увеличивает сопротивляемость к бубонной чуме. Поэтому после эпидемий «чёрной смерти» 1347 года доля этого генотипа выросла.
Мутация в гене CCR2 также уменьшает шанс проникновения ВИЧ в клетку и приводит к задержке развития СПИД.
Существует небольшой процент людей, в крови которых присутствует вирус, однако СПИД у них не развивается в течение долгого времени.
Обнаружено, что одним из главных элементов антивирусной защиты человека и других приматов является белок TRIM5a, способный распознавать капсид вирусных частиц и препятствовать размножению вируса в клетке. Данный белок у человека и других приматов имеет различия, которые обуславливают врожденную устойчивость шимпанзе к ВИЧ и родственным ему вирусам, а у человека — врожденную устойчивость к вирусу PtERV1 .
Другой важный элемент антивирусной защиты — интерферон-индуцируемый трансмембранный белок CD317/BST-2, получивший также название «tetherin» за его способность подавлять выделение вновь образовавшихся дочерних вирионов посредством их удержания на поверхности клетки. CD317 — трансмембранный белок 2го типа с необычной топологией — трансмембранный домен рядом с N-концом и гликозилфосфатидилинозитол на С-конце; между ними расположен внеклеточный домен. Показано, что CD317 непосредственно взаимодействует со зрелыми дочерними вирионами, «привязывая» их к поверхности клетки. Для объяснения механизма такого «привязывания» предложено четыре альтернативных модели, согласно которым две молекулы CD317 формируют параллельный гомодимер; один или два гомодимера связываются одновременно с одним вирионом и клеточной мембраной. При этом с мембраной вириона взаимодействуют либо оба мембранных «якоря» одной из молекул CD317, либо один из них. Спектр активности CD317 включает, по крайней мере, четыре семейства вирусов: ретровирусы, филовирусы, аренавирусы и герпесвирусы. Активность данного клеточного фактора ингибируется белками Vpu ВИЧ-1, Env ВИЧ-2 и SIV, Nef SIV, гликопротеином оболочки вируса Эбола и белком К5 герпесвируса саркомы Капоши. Обнаружен кофактор белка CD317 — клеточный белок ВСА2 — Е3 убиквитин-лигаза класса RING. BCA2 усиливает интернализацию вирионов ВИЧ-1, «привязанных» белком CD317 к клеточной поверхности, в CD63+ внутриклеточные везикулы с их последующим разрушением в лизосомах.
Просмотров: 21038
|
|
